



 Por Marinella Silva Laport, 21 de agosto de 2012
Por Marinella Silva Laport, 21 de agosto de 2012
Elevados níveis de resistência bacteriana têm sido relatados em todo o mundo e a procura por novos antibióticos de diversas fontes se faz necessária. Entre essas fontes estão os organismos marinhos, principalmente as esponjas, que apresentam uma grande diversidade de metabólitos secundários com atividades farmacológicas. O nosso grupo tem investigado esponjas marinhas com atividade antibacteriana sobre bactérias resistentes. Dez espécies de esponjas coletadas no litoral da cidade do Rio de Janeiro apresentaram atividade antibacteriana, sendo que o extrato aquoso da esponja Petromica citrina foi o que apresentou o maior espectro de ação. Assim, foi realizada uma caracterização química e biológica da substância bioativa de P. citrina e o seu modo de ação foi investigado em células de Staphylococcus aureus.
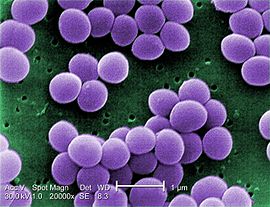 A atividade antibiótica do extrato aquoso foi determinada contra cerca de 60 estirpes tipo e clínicas resistentes a antibióticos. O extrato aquoso foi fracionado e a substância bioativa identificada por RMN e espectro de massa. O extrato aquoso foi ativo sobre a maioria das bactérias testadas, incluindo estirpes resistentes a antibióticos, como Enterococcus faecalis, S. aureus (MRSA), S. epidermidis, Mycobacterium abscessus subsp. bolletiie Neisseria gonorrhoeae.O extrato aquoso foi fracionado e o trisulfato de halistanol (isolado pela primeira vez a partir de P. citrina) foi identificado como sendo a principal substância bioativa. O trisulfato de halistanol tem um efeito bactericida sobre as células de S. aureus (CMI = 512 mg/L). Aparentemente, essa substância age sobre a membrana citoplasmática de S. aureus causando a lise celular. Esse antibiótico também apresentou toxicidade moderada contra as células eucarióticas L929 (fibrossarcoma). Esse trabalho demonstra que a esponja P. citrina tem um grande potencial antibacteriano, sendo uma fonte de substâncias e até para um protótipo de medicamento, para o tratamento de infecções causadas por bactérias resistentes.
A atividade antibiótica do extrato aquoso foi determinada contra cerca de 60 estirpes tipo e clínicas resistentes a antibióticos. O extrato aquoso foi fracionado e a substância bioativa identificada por RMN e espectro de massa. O extrato aquoso foi ativo sobre a maioria das bactérias testadas, incluindo estirpes resistentes a antibióticos, como Enterococcus faecalis, S. aureus (MRSA), S. epidermidis, Mycobacterium abscessus subsp. bolletiie Neisseria gonorrhoeae.O extrato aquoso foi fracionado e o trisulfato de halistanol (isolado pela primeira vez a partir de P. citrina) foi identificado como sendo a principal substância bioativa. O trisulfato de halistanol tem um efeito bactericida sobre as células de S. aureus (CMI = 512 mg/L). Aparentemente, essa substância age sobre a membrana citoplasmática de S. aureus causando a lise celular. Esse antibiótico também apresentou toxicidade moderada contra as células eucarióticas L929 (fibrossarcoma). Esse trabalho demonstra que a esponja P. citrina tem um grande potencial antibacteriano, sendo uma fonte de substâncias e até para um protótipo de medicamento, para o tratamento de infecções causadas por bactérias resistentes.
Referência:
Marinho PR, Simas NK, Kuster RM, Duarte RS, Fracalanzza SE, Ferreira DF, Romanos MT, Muricy G, Giambiagi-Demarval M, Laport MS. Antibacterial activity and cytotoxicity analysis of halistanol trisulphate from marine sponge Petromica citrina. J Antimicrob Chemother. 2012 In press.
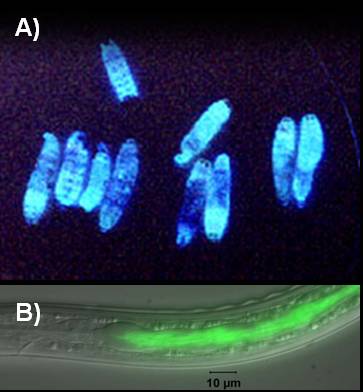 Laboratório de biologia de anaeróbios
Laboratório de biologia de anaeróbios
Por Leandro A. Lobo e Regina M.C.P. Domingues
A maneira como micro-organismos e seus hospedeiros se associam pode oscilar radicalmente, desde uma interação benéfica de mutualismo, em que a interação entre esses dois organismos pode ser tão íntima a ponto de um não viver sem o outro, até o parasitismo, em que um micro-organismo se beneficia em detrimento do organismo hospedeiro. Em um artigo publicado na revista Science em julho de 2012, Somvanchi e colaboradores analisaram a fundo a interação de simbiose entre a bactériaPhotorhabdus luminescens e o nematóide Heterorhabditis bacteriophora, que juntos infectam, matam e se reproduzem em insetos hospedeiros. A bactéria na sua forma mutualistica (forma M) é verticalmente transmitida para as formas juvenis do nematóide em desenvolvimento dentro do nematóide adulto e as coloniza graças à expressão de uma proteína filamentosa de superfície, a fimbria Mad (maternal adhesion). Quando as formas jovens infecciosas (JI) do nematóide colonizam o inseto hospedeiro, essas bactérias são regurgitadas e se multiplicam produzindo toxinas inseticidas. O cadáver do inseto passa a ser utilizado pelo nematóide como fonte de nutrientes e abrigo. No inseto, essas bactérias também produzem proteínas (CipA e CipB) ricas em aminoácidos essenciais indispensáveis para o crescimento do nematóide e antimicrobianos que evitam que microrganismos concorrentes se multipliquem na carcaça do inseto. Nesse estágio, as bactérias se encontram na sua forma patogênica (forma P). Surpreendentemente, as diferenças entre as formas M e P da bactéria se devem a uma simples inversão do promotor bacteriano que controla a expressão do locus Mad. Esse controle do tipo liga/desliga é mediado por uma invertase bacteriana chamada MadO e ocorre de forma estocástica. Nesse artigo, os autores manipulam geneticamente uma cepa dePhotorhabdus luminescens de forma que esta permaneça “travada” na forma M ou P. Análises fenotípicas demonstraram que a bactéria na forma mutualista (M) possui menores dimensões, crescimento mais lento, capacidade limitada de produção de diversas antimicrobianos, enzimas e proteínas importantes na infecção do inseto e consequentemente uma virulência reduzida em um modelo de infecção em larvas de Galleria mellonella (uma espécie de mariposa). Apesar de prevalente no nematóide adulto e da óbvia vantagem adaptativa das formas P, as formas M são preferencialmente transmitidas à prole graças à expressão da adesina Mad. À medida que o nematóide amadurece, as formas P prevalecem. Quando alcança a forma juvenil infecciosa, já esta “armada” para o combate com o inseto hospedeiro.
É interessante notar que bactérias da espécie Bacteroides fragilis, que fazem parte da microbiota intestinal humana controlam a expressão de um dos seus mais importantes fatores de virulência, a cápsula polissacarídica, de forma similar. Estruturalmente, esses polissacarídeos compõem um complexo iônico de moléculas referido como Complexo Polissacarídico Capsular (CPC) que é capaz de induzir a formação de abscessos intra-abdominais em animais de experimentação. Em 2001, Krinos e colaboradores demonstraram que a espécie é capaz de modular seus antígenos de superfície pela expressão de até oito polissacarídeos capsulares distintos (PSA-PSH) através de um mecanismo do tipo “liga – desliga” de promotores contendo inversões reversíveis de segmentos de DNA. Isto quer dizer que a espécie é capaz de exibir uma ampla combinação de polissacarídeos de superfície, o que pode ter grande implicação na sua manutenção no hospedeiro, seja em sítios infecciosos ou em populações de microbiota. Apesar do inquestionável papel do CPC na patogênese das infecções causadas por B. fragilis, recentemente foi verificado que o polissacarídeo A (PSA) ajuda a proteger o hospedeiro de doenças inflamatórias intestinais (MAZMANIAN, ROUND & KASPER, 2008).
O artigo de Somvanshi e colaboradores descreve, de forma elegante, como um processo aleatório e extremamente simples de regulação gênica pode promover mudanças marcantes na fisiologia celular de Photorhabdus luminescens e na sua interação de parasitismo/cooperação em diferentes hospedeiros. Mas não devemos esquecer que nós mesmos vivemos uma íntima e dinâmica associação com milhares de espécies bacterianas da nossa microbiota que possuem mecanismos de regulação gênica extramente semelhantes ao descrito em P. luminescens. De forma similar, o balanço entre agressão e cooperação na nossa microbiota está em constante mudança, evidenciando a importância e fragilidade desse tipo de interação.
Referências:
SOMVANSHI VS, SLOUP RE, CRAWFORD JM, MARTIN AR, HEIDT AJ, KIM KS, CLARDY J, CICHE TA. A single promoter inversion switches Photorhabdus between pathogenic and mutualistic states.Science. 2012 Jul 6;337(6090):88-93
KRINOS, C.M.; COYNE, M.J.; WEINACHT, K.G.; TZIANABOS, A.O.; KASPER, D.L. & COMSTOCK, L.E. Extensive surface diversity of a commensal microorganism by multiple DNA invertions. Nature, 414, 555-558, 2001.
MAZMANIAN, S.K.; ROUND, J.L. & KASPER, D.L. A microbial symbiosis factor prevents intestinal inflammatory disease. Nature, 453, 620-625, 2008.
 Por Raquel Regina Bonelli
Por Raquel Regina Bonelli
O autismo regressivo é caracterizado pelo início tardio, em que a criança se desenvolve normalmente até cerca de 18 meses e depois começa a evoluir para um comportamento típico de autista com sintomas como diminuição da capacidade de linguagem e de socialização. Estima-se que cerca de um terço dos autismos diagnosticados nos dias de hoje sejam desse tipo.
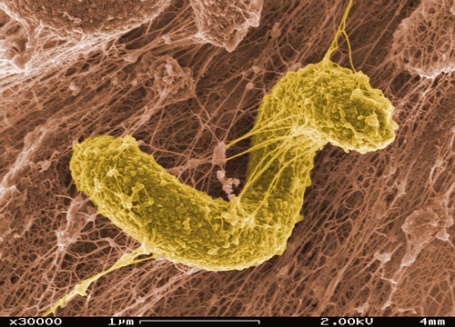
Ainda que esse seja um quadro eminentemente neurológico, pesquisas recentes apontam indícios de que a microbiota intestinal pode estar relacionada com o desenvolvimento de autismo regressivo. É o que autores americanos defendem em um artigo recentemente publicado na revistaAnaerobe, em que são apresentadas três evidências experimentais dessa correlação. A primeira evidência foi obtida ainda no início dos anos 2000, em que o uso de um antibiótico com ação sobre algumas espécies de bactérias que vivem no trato intestinal levou à diminuição nos sintomas comportamentais do autismo durante o tratamento. A suspensão do uso de antibiótico refletiu na regressão das melhorias obtidas. Alguns anos depois, com o advento de técnicas de identificação que não dependem de cultivo bacteriano, foi observado que, de uma forma geral, há variações importantes nos gêneros de bactérias prevalentes na microbiota de crianças com autismo avançado em relação às demais crianças. Por fim, um gênero específico de bactérias foi identificado como potencialmente importante no desenvolvimento de autismo. Estes microrganismos estariam causando dano de tecido por produzir um metabólito tóxico ou ainda utilizar componentes da dieta que seriam essenciais para o desenvolvimento da criança.
Assim, em ultima instância, fatores genéticos (como perfil de susceptibilidade imunológica) e ambientais (como dieta e uso de antimicrobianos) podem contribuir para as causas do autismo regressivo através da influência na microbiota intestinal. Muito há que se evoluir ainda na compreensão da patogênese desse quadro, mas sem dúvida, quanto mais a ciência puder compreender as causas do autismo, mais eficientes serão também as estratégias de tratamento e prevenção desta doença.
