



Por: Olinda Cabral da Silva Santos
As doenças infecciosas causadas por bactérias, fungos, vírus e parasitas ainda constituem o principal problema de saúde pública. Seu impacto é particularmente maior em países em desenvolvimento, devido à precariedade dos sistemas de saúde, uso indiscriminado de antimicrobianos e emergência de microrganismos multirresistentes.
A resistência aos antimicrobianos é uma preocupação mundial e crescente. O Brasil e os países latino-americanos, em geral, apresentam níveis mais elevados de resistência bacteriana quando comparados com a Europa e os Estados Unidos, principalmente entre cocos Gram-positivos e bacilos Gram-negativos, incluindo os não--fermentadores e as enterobactérias produtoras de β-lactamases de espectro estendido (extended-spectrum β-lactamase – ESBL).
Os produtos naturais constituem uma das principais fontes de novos agentes terapêuticos para várias doenças, incluindo as infecciosas. Somente uma pequena porção da diversidade disponível de fungos, da fauna e flora marinhas, de bactérias e de plantas tem sido explorada, e sugere-se que recursos ilimitados podem ser obtidos através do estudo desses organismos.
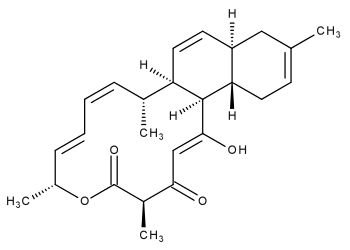
Um exemplo promissor desta última assertiva é o novo antibiótico antracimicina (Figura 1), produzido pela estirpe Streptomyces halstedii CNH365, isolada a partir de sedimentos marinhos coletados na costa da Califórnia. A antracimicina é uma substância tricarbocíclica pertencente à classe dos policetídeos, e a sua estrutura química única poderia levar ao desenvolvimento de uma nova classe de antibióticos.
Atualmente, o seu maior risco está associado à utilização dos esporos como arma de guerra biológica e no bioterrorismo. Em 2001, uma semana após o ataque ao World Trade Center, um grupo terrorista 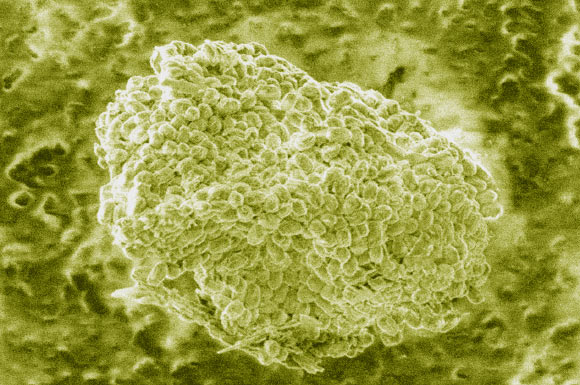 enviou envelopes contendo esporos de B. anthracis para diferentes localidades dos Estados Unidos. Esta ação resultou em 22 casos de antraz confirmados, incluindo cinco mortes por antraz pulmonar. Dada a gravidade desta doença, aliado ao fato dos esporos poderem ser dispersos na forma de aerossóis, o desenvolvimento de novos agentes antibióticos para o tratamento desta infecção vem se tornando um objetivo prioritário para os Estados Unidos.A antracimicina apresentou potente atividade inibitória contra Bacillus anthracis em uma concentração mínima inibitória (CMI) de 0,031 µg/ml. Este microrganismo é o agente etiológico do carbúnculo hemático, também conhecido como antraz. Normalmente, o antraz afeta mamíferos herbívoros, principalmente bovinos, equinos e caprinos, podendo casualmente contaminar o homem pelo contato com animais ou materiais infectados. De acordo com a via em que os esporos (Figura 2) foram contraídos, a infecção apresenta três diferentes formas de contágio: cutânea (manifestação mais comum), inalatória (letal em 95% dos casos) e gastrointestinal.
enviou envelopes contendo esporos de B. anthracis para diferentes localidades dos Estados Unidos. Esta ação resultou em 22 casos de antraz confirmados, incluindo cinco mortes por antraz pulmonar. Dada a gravidade desta doença, aliado ao fato dos esporos poderem ser dispersos na forma de aerossóis, o desenvolvimento de novos agentes antibióticos para o tratamento desta infecção vem se tornando um objetivo prioritário para os Estados Unidos.A antracimicina apresentou potente atividade inibitória contra Bacillus anthracis em uma concentração mínima inibitória (CMI) de 0,031 µg/ml. Este microrganismo é o agente etiológico do carbúnculo hemático, também conhecido como antraz. Normalmente, o antraz afeta mamíferos herbívoros, principalmente bovinos, equinos e caprinos, podendo casualmente contaminar o homem pelo contato com animais ou materiais infectados. De acordo com a via em que os esporos (Figura 2) foram contraídos, a infecção apresenta três diferentes formas de contágio: cutânea (manifestação mais comum), inalatória (letal em 95% dos casos) e gastrointestinal.
A antracimicina também foi capaz de inibir o crescimento de Staphylococcus aureus resistente à meticilina (methicillin-resistant S. aureus – MRSA), em uma CMI de 0,062 µg/ml. Esta bactéria é responsável por infecções primárias da corrente sanguínea, infecções de pele e tecidos moles e infecções no trato respiratório inferior. Estirpes de MRSA adquiriram prevalência expressiva nas opulações adulta e pediátrica em ambiente hospitalar, sendo encontradas nos hospitais brasileiros com variações entre 30% e 60%.
O clone responsável pela maioria das infecções por MRSA no Brasil, chamado clone epidêmico brasileiro (Brazilian epidemic clone – BEC), apresenta resistência a múltiplas drogas. Clindamicina, sulfametoxazol-trimetoprima, ciprofloxacina e gentamicina são ativos contra MRSA-BEC a uma taxa menor do que 10%, restando como alternativa terapêutica para as infecções graves causadas por estas bactérias o uso dos antibióticos glicopeptídicos (teicoplanina e vancomicina), das estreptograminas (quinupristina/dalfopristina), das oxazolidinonas (linezolida) e dos lipopeptídeos cíclicos (daptomicina).
Além das bactérias anteriormente citadas, a antracimicina também foi capaz de inibir outros patógenos Gram-positivos, tais como Enterococcus faecalis (CMI = 0,125 µg/ml) e Streptococcus pneumoniae (CMI = 0,25 µg/ml). Por outro lado, esta droga se mostrou pouco efetiva contra bactérias Gram-negativas, apresentando CMIs entre > 128 e > 256 µg/ml. A síntese de um análogo da antracimicina, a dicloro-antracimicina, demonstrou que a adição de cloro à estrutura aumentou a habilidade do composto em penetrar na parede celular de bactérias Gram-negativas. A dicloro-antracimicina foi ativa contra Haemophilus influenzae, Burkholderia thailandensis, Escherichia coli e Pseudomonas aeruginosa, com CMIs variando entre 4 e 32 µg/ml.
Embora o mecanismo de ação não tenha sido totalmente elucidado, resultados obtidos a partir de experimentos de marcação metabólica indicaram que a antracimicina atua inibindo a síntese de DNA e de RNA. Além disso, estudos preliminares in vivo demonstraram que esta substância foi capaz de conferir significativa proteção (90% de sobrevivência) em camundongos CD1 infectados com MRSA.
O último antibiótico isolado a partir de fontes naturais foi a daptomicina, em 1986. Este composto, produzido por uma estirpe de Streptomyces roseosporus, pertence à classe dos lipopeptídeos cíclicos e foi aprovado para o tratamento de infecções causadas por bactérias Gram-positivas em 2003.
O estudo apresentado acima foi desenvolvido pelo grupo do Professor William Fenical, do Instituto Scripps de Oceanografia (California, USA), e publicado no periódico científico alemão Angewandte Chemie. O isolamento da antracimicina indica que o ambiente marinho, que representa cerca de metade da diversidade global, constitui uma rica fonte que precisa ser explorada visando o desenvolvimento de novos agentes antimicrobianos para compor o arsenal terapêutico contra microrganismos multirresistentes.
Bibliografia:
Eliopoulos, G.M., Willey, S., Reiszner, E., Spitzer, P.G., Caputo, G. & Moellering, R.C. In vitro and in vivo activity of LY146032, a new cyclic lipopeptide antibiotic. Antimicrob. Agents Chemother., 30(4), 532-535, 1986.
Fauci, A.S. & MORENS, D.M. The perpetual challenge of infectious diseases. N. Engl. J. Med., 366(5), 454-61, 2012.
Jang, K.H., Nam, S.J., Locke, J.B., Kauffman, C.A., Beatty, D.S., Paul, L.A. & Fenical, W. Anthracimycin, a potent anthrax antibiotic from a marine-derived actinomycete. Angew. Chem. Int. Ed., 52, 7822-7824, 2013.
Newman, D.J. & Cragg, G.M. Natural products as sources of new drugs over the 30 years from 1981 to 2010. J. Nat. Prod., 75, 311-335, 2012.
Rossi, F. The challenges of antimicrobial resistance in Brazil. Clin. Infect. Dis., 52(9), 1138-1143, 2011.
Sweeney, D.A., Hicks, C.W., Cui, X., Li, Y. & Eichacker, P.Q. Anthrax Infection. Am. J. Respir. Crit. Care Med., 184(12), 1333-1341, 2011.
Por: Maria do Carmo de Freire Bastos
Extensas perdas econômicas associadas à agricultura são derivadas de doenças causadas por microrganismos em plantas de importância agronômica. Essas doenças têm como importantes agentes bactérias e fungos fitopatogênicos.
As medidas de controle dessas infecções geralmente envolvem o uso extensivo de pesticidas. Entretanto, tal estratégia apresenta diversas desvantagens, entre as quais vale a pena destacar os custos desse tratamento para o agricultor, a seleção de microrganismos resistentes aos pesticidas empregados e os riscos ambientais oriundos do acúmulo dessas substâncias no solo. Por isso, outra forma de se evitar tais infecções envolve a obtenção de plantas carreando genes naturais de resistência aos fitopatógenos. Entretanto, dependendo da planta, esta estratégia possui uso limitado devido à escassez desses genes de resistência naturais e ao longo período necessário para o cruzamento de plantas relacionadas, isto é, sexualmente compatíveis. Assim sendo, outra possibilidade hodierna que se tem mostrado bastante promissora é a obtenção de plantas carreando genes codificadores de peptídeos antimicrobianos de amplo espectro de ação (PAMs).
Os PAMs são produzidos por uma variedade de organismos procarióticos e eucarióticos, incluindo-se microrganismos, plantas, animais invertebrados e vertebrados (Quadro 1). Eles são considerados parte integrante da imunidade inata e a primeira linha de defesa das células contra microrganismos invasores (Jenssen et al., 2006). A maioria desses PAMs é catiônica e hidrofóbica a age ao nível da membrana citoplasmática das células-alvo, levando-as à morte. Entretanto, alguns desses PAMs possuem outros sítios-alvo de ação, como a parede celular, hidrolisando-a.
PAMs de diversas origens têm sido utilizados para a obtenção de plantas transgênicas. As plantas transgênicas são definidas como aquelas plantas carreando novos genes, oriundos de outras plantas, relacionadas ou não, de microrganismos ou de animais. A introdução desses genes nessas plantas é realizada por meio de experimentos de transformação, que, neste caso, representa a implantação de novos genes por mecanismos moleculares que não envolvem cruzamento e fecundação.
Quadro 1. Alguns exemplos de PAMs produzidos por organismos eucarióticos e procarióticos.
| Organismo Produtor | PAMs |
| Mamíferos | Defensivas, protegrina |
| Anfíbios | Magainina, bombinina, demaseptinas |
| Insetos | Defensinas, cecropinas, melitina |
| Plantas | Defensinas, tioninas, AP24 |
| Bactérias | Bacteriocinas |
As etapas para o desenvolvimento de uma planta transgênica incluem:
1. Seleção do gene de interesse;
2. Clonagem do gene em um vetor de expressão em eucarioto;
3. Transformação da planta escolhida com o vetor recombinante;
4. Integração do gene de interesse ao genoma da planta;
5. Seleção das plantas transformadas;
6. Expressão do gene de interesse e
7. Transmissão do gene aos descendentes.
Como exemplo, iremos abordar a obtenção de plantas transgênicas simples, duplas ou triplas de um cultivar de batata (Solanum tuberosum cv. Spunta), carreando os genes estruturais dos PAMs dermaseptina, lisozima e AP24, descrita no trabalho publicado por Rivero e colaboradores (2012). As características dos três PAMs estão sumarizadas no Quadro 2. Para a obtenção das plantas transgênicas, foi empregada a técnica de transformação baseada na utilização dos plasmídeos Ti (Kado, 1993).
Quadro 2. Características dos PAMs empregados para a obtenção de plantas transgênicas de Solanum tuberosum cv. Spunta.
| PAM | Fonte | Tamanho | Alvo de Ação | Microrganismos-alvo |
| dermaseptina | sapo | 28 a 34aa | membrana citoplasmática |
bactérias, fungos filamentosos, leveduras e protozoários |
| AP24 | Tabaco | cerca de 210aa | ||
| ovo de galinha | 129aa | parede celular | bactérias |
aa, ácidos aminados
Plasmídeos Ti
Os plasmídeos Ti (de indução de tumor) são megaplasmídeos de cerca de 200 kb encontrados em algumas estirpes de Agrobacterium tumefaciens, uma bactéria Gram-negativa encontrada no solo (Kado, 1993; Schröder & Lanka, 2005). Em sua organização genética, os plasmídeos Ti possuem duas regiões muito importantes para a formação de tumores nas plantas (Figura 1):
1. Região do DNA T. Esta região tem cerca de 25 kb e é ladeada por repetições diretas de 25 pb, chamadas bordos direito e esquerdo, e contém genes estruturais codificadores de auxinas e citocininas (ambas representando hormônios de crescimento vegetal) e de opinas (que são ácidos aminados condensados a açúcares), entre as quais predominam a octopina ou a nopalina. É esta região do DNA T que o A. tumefaciens é capaz de transferir para as plantas, gerando a formação de tumores.
2. Região vir. Esta região tem cerca de 35 kb e 25 genes vir (de virulência), agrupados em seis ou sete operons. Estes genes codificam todas as proteínas necessárias à formação de um canal intermembrana, entre a bactéria e a célula vegetal, e à transferência do DNA T para esta célula.
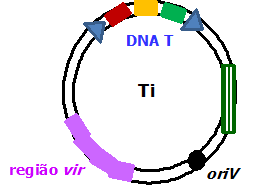
Figura 1. Esquema simplificado dos plasmídeos Ti, mostrando a região vir e a região do DNA T. Os triângulos azuis representam os bordos direito e esquerdo, os retângulos vermelho, amarelo e verde representam, respectivamente, os genes estruturais das auxinas, citocininas e opinas, e o retângulo verde riscado representa os genes envolvidos no catabolismo das opinas. Os vários plasmídeos Ti diferenciam-se, entre outros aspectos, pelo tipo de opina codificado e pelos genes responsáveis pelo seu catabolismo.
Quando o DNA T é transferido para a planta (somente uma das fitas do DNA é transferida), após contato celular estabelecido entre a bactéria e a célula vegetal (Figura 2), este DNA é transportado para o núcleo da célula, onde o DNA T se integra a um dos cromossomos, de uma forma randômica. Como os genes das auxinas, das citocininas e das opinas possuem promotores eucarióticos, após a integração, eles podem se expressar. A síntese das auxinas e das citocininas leva a uma multiplicação descontrolada das células vegetais, resultando na formação de tumores nas plantas. Já as opinas produzidas serão excretadas pelas células tumorais e servirão de fonte de C e de N para a nutrição bacteriana.
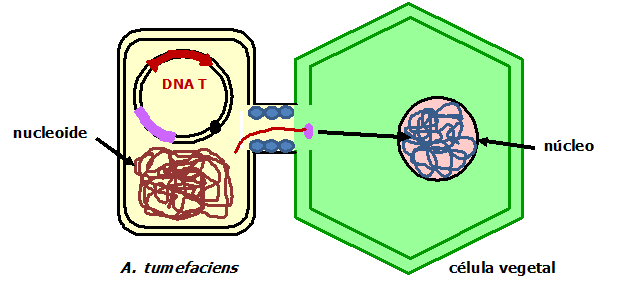
Figura 2. Esquema simplificado da transferência de uma fita do DNA T do plasmídeo Ti para a planta. A fita do DNA T é liberada do plasmídeo mediante a ação principal de duas proteínas Vir (VirD1 e VirD2), sendo que VirD2 () permanece covalentemente ligada ao extremo 5’ P da fita T liberada). Em seguida, a fita T é transferida para a célula vegetal mediante a formação de um canal intermembrana, ligando as duas células, formado por várias proteínas Vir (compondo um sistema de secreção do tipo 4). Uma vez no citoplasma da célula vegetal, a fita T é transferida para o núcleo, mediante a participação de proteínas Vir e de proteínas vegetais envolvidas em localização nuclear, e depois se integra a um cromossomo, passando a expressar os genes nela contidos.
Obtenção das plantas transgênicas contendo os genes estruturais de PAMs
Inicialmente, os genes codificadores da dermaseptina (De), da lisozima (Ly) e do AP24 (Ap) foram, separadamente, clonados em vetores de expressão apropriados. A clonagem foi feita dentro da região do DNA T, sendo que os genes dos hormônios de crescimento e da opina foram substituídos pelo gene de interesse, como mostrado na Figura 3. Os plasmídeos recombinantes gerados (pDe, pLy, pAp e pApLy) foram introduzidos no cultivar de batata escolhido (Spunta) por meio de transformação binária (Murai, 2013).
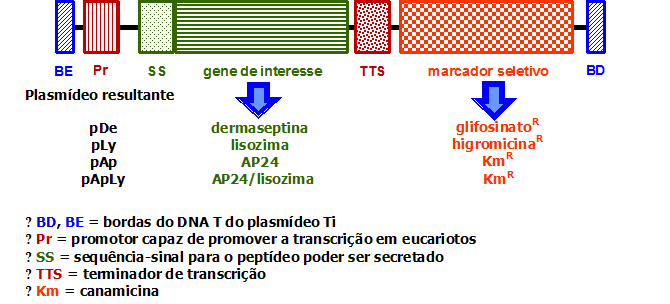
Figura 3. Características das sequências de DNA clonadas, carreando os genes estruturais codificadores de PAMs.
Na transformação binária, a planta é infectada por uma estirpe de A. tumefaciens carreando dois plasmídeos: um plasmídeo Ti, com deleção (D) de toda a região do DNA T, mas portador da região vir, e o plasmídeo recombinante contendo o gene de interesse e um gene marcador clonados na região do DNA T modificada, que só conserva os bordos direito e esquerdo. Os genes vir localizados no plasmídeo DTi irão promover a liberação da fita T, localizada no plasmídeo recombinante, e a sua transferência para as células vegetais. No caso da batata, foram empregados discos de minitubérculos para a infecção. Assim sendo, quando em contato com esses discos, a estirpe de A. tumefaciens pôde transferir o gene de interesse e o gene marcador para as células vegetais, mas não pôde mais causar a formação de tumores. Após a infecção, os minitubérculos foram, então, transferidos para um meio de cultivo adequado contendo o agente seletivo apropriado (glifosinato, higromicina ou canamicina). Após cerca de três semanas, foram obtidas plântulas resistentes aos agentes seletivos, que foram, então, crescidas em frascos com meio de cultura e, depois, transferidas para vasos com solo estéril, gerando as “explantas” (plantas derivadas de transformação).
A confirmação da presença dos genes de interesse nas “explantas” foi feita por PCR, empregando-se DNA extraído das folhas. A planta transgênica contendo o gene De foi, posteriormente, retransformada com o plasmídeo recombinante pApLy, gerando uma planta transgênica tripla, DeApLy, resistente ao glifosinato e à canamicina.
Os cinco tipos de plantas transgênicas (De, Ly, Ap, ApLy e DeApLy) foram testados quanto à resistência a cinco fitopatógenos de batateiras: duas espécies de bactérias (Erwinia caratovora eStreptomyces scabies) e três espécies de fungos (Phytophthora infestans, Rhizoctonia solani e Fusarium solani), empregando-se diferentes modelos de infecção: broto axial, folhas ou tubérculos. Os resultados obtidos estão sumarizados no Quadro 3.
++++, resistência >80%; +++, resistência entre 61 e 80%; ++, resistência entre 41 e 60%; +, resistência entre 21 e 40%; ±, resistência entre 5 e 20%; -, resistência <5%. Este nível de resistência foi determinado em função do número de plantas ou tubérculos testados (geralmente, em torno de 60 plantas ou tubérculos por tipo, oriundos de três experimentos independentes) que apresentaram sintomas e da gravidade dos sintomas observados: necrose, crestamento, clorose ou podridão.
Baseando-se nos experimentos realizados, pôde-se concluir:
● que as plantas transgênicas De, Ly, ApLy e DeApLy exibiram um alto nível de resistência aos patógenos bacterianos;
● que o nível de resistência aos fungos variou dependendo do gene presente na planta transgênica ou da combinação desses genes;
● que as plantas transgênicas duplas ou triplas foram as que exibiram um maior nível de resistência aos cinco patógenos testados, que são muito frequentes nas áreas de cultivo de batatas.
Os resultados aqui resumidos indicam que PAMs podem funcionar como uma nova fonte de resistência das plantas a um amplo grupo de fitopatógenos, podendo ser utilizados na prevenção de doenças de impacto econômico. Entretanto, embora os resultados apresentados neste trabalho sejam bastante promissores, demonstrando, de forma inequívoca, o potencial biotecnológico de PAMs também na agricultura, a efetividade dessas substâncias produzidas plantas transgênicas precisa ainda ser comprovada em experimentos de campo, em diferentes ecossistemas agrários, onde ocorre a interferência de fatores abióticos e bióticos, não levados em consideração nos experimentos realizados em condições ambientais controladas e em solo ou meio de cultivo estéril.
Referências:
Jenssen, H., Hamill, P. & and Hancock, R.E.W. 2006. Peptide antimicrobial agents. Clin. Microbiol. Rev., 19: 491-511.
Kado, C.I. 1993. Agrobacterium-mediated transfer and stable incorporation of foreign genes in plants. In: Bacterial Conjugation. Edited by D.B. Clewell, Plenum Press, New York, pp. 243-254.
Murai, N. 2013. Plant binary vectors of Ti plasmid in Agrobacterium tumefaciens with a broad host-range replicon of pRK2, pRi, pSa or pVS1. Am. J. Plant Sci., 4: 932-939.
Rivero, M., Furman, N., Mencacci, N., Picca, P., Toum, L., Lentz, E., Bravo-Almonacid, F. & Mentaberry, A. 2012. Stacking of antimicrobial genes in potato transgenic plants confers increased resistance to bacterial and fungal pathogens. J. Biotechnol., 157: 334-343.
Schröder, G. & Lanka, E. 2005. The mating pair formation system of conjugative plasmids - A versatile secretion machinery for transfer of proteins and DNA. Plasmid, 54: 1-25.
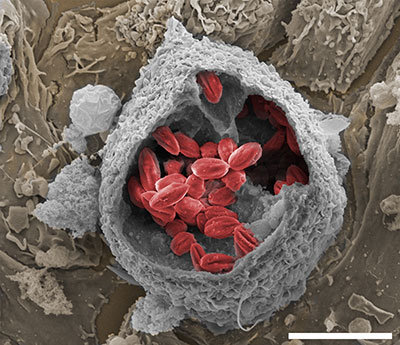 Imagem ampliada 7.500 vezes mostra as bolsas (vacúolos) formados pelo protozoário L. amazonensis (vermelho), agente causador da leishmaniose cutânea, dentro de macrófago de camundongo (cinza). FOTO Fernando Real/CNPQ
Imagem ampliada 7.500 vezes mostra as bolsas (vacúolos) formados pelo protozoário L. amazonensis (vermelho), agente causador da leishmaniose cutânea, dentro de macrófago de camundongo (cinza). FOTO Fernando Real/CNPQ
Pesquisadores da Escola Paulista de Medicina da Universidade Federal de São Paulo (Unifesp) identificaram novas pistas de como o parasita causador da leishmaniose invade as células de defesa do organismo e, uma vez no interior delas, retarda a ativação do arsenal imunológico que deveria eliminá-lo. O grupo coordenado pela bióloga Diana Bahia sequenciou o material genético do protozoário Leishmania amazonensis – espécie encontrada predominantemente na Amazônia que provoca uma forma mais rara e deformante de leishmaniose cutânea – e comparou com o de uma espécie-irmã, exclusiva da América Central, também marcada pelo desenvolvimento de lesões na pele semelhantes às da hanseníase. Um dos objetivos era identificar os genes, e consequentemente as proteínas por eles codificadas, que permitiriam ao parasita viver camuflado no interior das células de defesa, sem prejudicar o hospedeiro.
Usando ferramentas de bioinformática, os pesquisadores chegaram a duas proteínas candidatas a explicar por que o parasita consegue conviver harmoniosamente com as células que deveriam matá-lo. Essas proteínas pertencem à classe das chamadas heat-shock proteins, que também são produzidas pelo hospedeiro do parasita – em geral, roedores e seres humanos. Em colaboração com grupos do Laboratório Nacional de Biociências (LNBio) e do Laboratório de Genômica e Expressão da Universidade Estadual de Campinas, a equipe obteve indícios de que a proteína fabricada e liberada pelo protozoário parece imitar a do hospedeiro. Os pesquisadores suspeitam que essa imitação permitiria a ligação dessas proteínas a componentes do arsenal imunológico do indivíduo infectado, bloqueando sua ativação e silenciando a resposta inflamatória.
O estudo também investigou que genes estariam relacionados à formação de uma bolsa que abriga o parasita no interior dos macrófagos, as células de defesa que os englobam e tentam destruí-los. Nela, o parasita se multiplica e resiste a eventuais ataques do sistema imunológico. No caso da L. amazonensis e da sua espécie-irmã, a L. mexicana, essa bolsa é bem mais espaçosa do que as formadas por outras espécies de protozoários causadores da leishmaniose. “Essa pode ser uma das maneiras de o parasita subverter e enganar o sistema imunológico do hospedeiro”, conta Fernando Real, pesquisador da Unifesp e um dos autores principais do estudo que descreveu esses resultados na edição de julho da revista DNA Research.
De acordo com os pesquisadores, juntas, essas estratégias também permitiriam ao parasita viver camuflado no organismo infectado, sem desencadear os sintomas que se manifestam em pessoas com o sistema imunológico fragilizado. “Essas duas espécies deLeishmania desenvolveram estratégia para viver silenciosamente em hospedeiros vertebrados”, conta Diana. Para ela, essa convivência, pacífica especialmente para o parasita, é resultado de um longo processo evolutivo em que a morte do hospedeiro não seria vantajosa para o protozoário. “A investigação dos fatores relacionados a essa interação durável pode ser útil para entendermos como o parasita se estabelece no ser humano”, diz.
As suspeitas dos pesquisadores ainda precisam ser comprovadas experimentalmente. Um dos próximos passos agora é isolar as bolsas (vacúolos) formadas por essa espécie de Leishmania e tentar mapear seus componentes. Esse mapeamento dependia das informações do genoma da L. amazonensis, agora sequenciado e disponibilizado para a comunidade científica. “O genoma abre mais portas do que fecha”, afirma Diana. “Temos mais perguntas para investigar”.
O estudo foi financiado pela FAPESP e pelo Conselho Nacional de Desenvolvimento Científico e Tecnológico (CNPq).
Projetos
1. Identificação e caracterização molecular de proteínas quinases de Trypanosoma cruzi para o estudo da comunicação celular, modelagem molecular e desenho de drogas inibidoras: estudo dos parceiros das vias de sinalização focado na invasão de EA (2007/50551-2); Modalidade Auxílio à Pesquisa – Apoio a Jovens Pesquisadores;Coord. Diana Bahia/Unifesp; Investimento R$ 532.652,38 (FAPESP).
2. Estudo dos mecanismos de fusão entre vacúolos parasitóforos heterotípicos de Leishmania spp. (2010/19335-4); Modalidade Bolsa de pós-doutorado; Coord.Renato Arruda Mortara/Unifesp; Investimento R$ 233.453,22 (FAPESP).
Artigo científico
REAL, F. et al. The genome sequence of Leishmania (Leishmania) amazonensis: functional annotation and extended analysis of gene models. DNA Research. v. 20, p. 1-15. jul. 2013.
Fonte: Revista Pesquisa - FAPESP
